(知识点)碱性酒石酸铜甲液的测定
1、直接滴定法
1)原理:样品去除蛋白质后,在加热条件下直接滴定校准后的碱性酒石酸铜溶液,还原糖将二价铜还原为氧化亚铜。 以亚甲蓝为指示剂,终点稍过量的还原糖将蓝色氧化亚甲蓝还原为无色还原亚甲蓝,根据样品消耗的体积计算还原糖含量。
直接滴定法已多次改进。 只要严格遵循实验条件,分析结果的准确性和重现性即可满足定量分析的要求。
2) 试剂
①斐林试剂溶液:称取15g硫酸铜(CuSO4·5H2O)和0.05g四甲基蓝,溶于水并稀释至1000ml。
②费林氏剂B:称取50g酒石酸钾钠和75g NaOH,溶于水,然后加入4g亚铁氰化钾,完全溶解后,用水稀释至1000ml,储存于带橡皮塞的玻璃瓶中。
③醋酸锌溶液:称取醋酸锌晶体21.9g,加冰醋酸3ml,加水溶解至100ml。
④106g/l亚铁氰化钾溶液。
⑤ 葡萄糖标准溶液:准确称取已于96±2℃干燥2小时的纯葡萄糖1.0000g,加水溶解,加5ml HCl,用水稀释至1000ml。 每1ml该溶液相当于1.0mg葡萄糖。
3)操作方法
①样品处理:准确称取2.5~5.0g样品(粉碎)置于250ml容量瓶中,加50ml水,摇匀后缓慢加入5ml醋酸锌溶液,混匀后缓慢加入5ml亚铁氰化物。 钾溶液,摇匀,加水至刻度,摇匀,静置30分钟,用干滤纸过滤,弃去初滤液,滤液备用。
②碱性酒石酸铜溶液的标定:取5.00ml碱性酒石酸铜A溶液和5.00ml碱性酒石酸铜B溶液,置于250ml锥形瓶中,加10ml水,加入3颗玻璃珠,从滴定管中加入约9ml标准品葡萄糖溶液在 2 分钟内加热至沸腾。 趁热继续以0.5滴/秒的速度滴加糖溶液,直至溶液颜色刚刚褪去为终点,记录消耗葡萄糖溶液的体积。 平行进行3次运算,得到m消耗的葡萄糖溶液的平均体积。
计算每10ml(A、B各5ml)碱性酒石酸铜溶液相当于葡萄糖的质量(mg),即
m=v×c
式中,m——10ml碱性酒石酸铜溶液相当于葡萄糖的质量(mg)
v——校准时消耗的葡萄糖标准溶液的总体积
c——葡萄糖标准溶液浓度(mg/ml)
③样品溶液的初步测定:取斐林溶液A和溶液B各5ml,置于150ml锥形瓶中,加入10ml水和2颗玻璃珠,控制在2分钟内加热至沸腾。 沸腾时,先快后慢地提高速度。 ,从滴定管中加入样品液,在沸腾的同时以0.5滴/秒的速度继续滴定至蓝色刚刚褪去,记录消耗样品液的体积。
④ 样品溶液的测定:取斐林溶液A和溶液B各5ml,置于150ml锥形瓶中,加10ml水和2颗玻璃珠,从滴定管中加入比规定体积少1ml的样品溶液,并静置 2 分钟。 加热至沸腾,在沸腾的同时以0.5滴/秒的速度继续滴定至蓝色刚刚消失,记录所消耗的样品溶液的体积。 同样的方法平行进行3次,求出消耗的样品液的平均体积。
4)结果计算
w(还原糖)=m1×100×250/(m×v×1000)=25×m1/(m×v)
式中:w(还原糖)——还原糖的质量分数(%)
m——样品的质量(g)
v——测量过程中消耗的样品溶液的平均体积(ml)
m1——10ml碱性酒石酸铜溶液相当于葡萄糖的质量(mg)
250——样品溶液总体积(ml)
5)说明
①采用醋酸锌、亚铁氰化钾作为蛋白质沉淀剂; 碱性酒石酸铜A、B溶液应分别配制和储存,不能提前混合储存。
②测量时的滴定速度、加热时间、热源稳定性、锥形瓶壁厚对测量精度影响较大。 预测和正式测量过程中的样本条件应保持一致。 平行测定的样品溶液消耗体积之差不应超过0.1ml。
③整个滴定过程应保持微沸状态,继续滴定结束时体积应控制在0.5~1ml以内,否则应重做。
④样品中还原糖的质量分数不宜过高或过低。 需要根据预测进行调整,0.1%比较合适。
⑤ 当滴定到达终点时,指示剂被还原糖还原,蓝色消失,变成淡黄色。 如果放置一段时间并暴露在空气中的氧气中,指示剂会被氧化并重新变成蓝色。 此时不应再进行滴定。
⑥ 配制标准溶液所用的葡萄糖应在50~60℃下干燥30分钟,然后放入98~100℃烘箱中至恒重。
⑦碱性酒石酸铜具有很强的氧化能力,既能氧化醛糖,又能氧化酮糖,因此测定总还原糖的质量。
⑧本方法定量糖的依据是碱性酒石酸铜溶液中Cu2+的量。 因此,样品处理过程中不能使用CuSO4和NaOH作为澄清剂,以免意外地将Cu2+引入样品溶液中而给出错误的结果。
⑨ 在碱性酒石酸铜B溶液中加入亚铁氰化钾,使生成的Cu2O红色沉淀与之形成可溶性无色络合物,使终点易于观察。
⑩亚甲蓝也是一种氧化剂,但在测量条件下其氧化能力比Cu2+弱。 因此,还原糖首先与Cu2+反应。 Cu2+完全反应后,稍过量的还原糖会与亚甲蓝反应。 溶液颜色消失,表明已达到终点。
2、高锰酸钾法
本方法为国家标准分析方法。 适用于各种食品中还原糖的测定,也适用于深色样品液体。 该方法的主要特点是准确度高、重现性好,均优于直接滴定法。 但操作复杂、耗时,需要高锰酸钾法专用的糖回收表(见附录)。
1)原理:还原糖与过量的碱性酒石酸铜溶液反应,还原糖将二价铜还原为氧化亚铜。 过滤后得到氧化亚铜,用Fe2(SO4)3溶液氧化溶解,将铁盐还原为亚铁盐,生成的亚铁盐用高锰酸钾标准溶液滴定。 根据高锰酸钾标准溶液的消耗量,计算出氧化亚铜的质量。 从附录中找出相当于氧化亚铜量的还原糖量,然后计算样品中还原糖的含量。
2) 试剂
①碱性酒石酸铜溶液:称取硫酸铜(CuSO4·5H2O)35.639g,加适量水溶解,加浓H2SO4 0.5ml,加水稀释至500ml,用精石棉过滤。
②碱性酒石酸铜B溶液:称取173g酒石酸钾钠和50g NaOH,加适量水溶解,稀释至500ml,用精制石棉过滤,贮存于带橡皮塞的玻璃瓶中。
③精制石棉:先将石棉浸泡在3mol/LHCl中2~3小时,然后用水清洗; 然后用100g/L NaOH溶液浸泡2~3小时,倒掉溶液,再用碱性酒石酸铜B溶液浸泡数小时,用水洗净。 ; 然后用3mol/LHCl浸泡数小时,用水洗至不再呈酸性。 然后加水摇匀,使其变成细浆状的柔软纤维。 将其浸泡在水中并存放在玻璃瓶中,该玻璃瓶可用于填充古什的坩埚。
④0.02mol/L高锰酸钾标准溶液:称取3.3g高锰酸钾,溶于1050ml水中。 慢慢煮20至30分钟。 冷却后,密封避光保存数天。 用垂直熔化漏斗过滤并储存。 棕色瓶子里。 用参比草酸钠校准其准确浓度。
⑤1mol/LNaOH溶液:称取4gNaOH,加水溶解并稀释至100ml。
⑥Fe2(SO4)3溶液:称取50gFe2(SO4)3,加200ml水溶解,缓慢加入100ml H2SO4,冷却后加水稀释至1000ml。
⑦3mol/LHCl:量取30ml浓HCl,加水稀释至120ml。
3)仪器
①25ml固始坩埚或G4立式坩埚。
②真空泵或液压真空管。

4) 测量方法
①来样加工
A、牛奶、乳制品、含蛋白质冷食:称取约2~5g固体样品(液体样品25~50ml)置于250ml容量瓶中,加入50ml水,摇匀加入碱性酒石酸铜溶液10ml和1mol/L NaOH溶液4ml至刻度,混匀,静置30分钟,用干滤纸过滤,弃去初滤液,滤液备用测量。
B、酒精饮料:取100ml样品,置于蒸发皿中,用1mol/L NaOH溶液中和至中性,蒸发至原体积的1/4,转移至250ml容量瓶中。 添加50毫升水并搅拌均匀。 接下来从A项“加入10ml碱性酒石酸铜溶液”开始,同样操作。
C、含淀粉较多的食品:称取样品10~20g,置于250ml容量瓶中,加水200ml,在45℃水浴中加热1小时,不时摇匀。 冷却后,加水至刻度,搅拌均匀,静置。 放。 取20ml上清液置于另一个250ml容量瓶中。 接下来从A项“加入10ml碱性酒石酸铜溶液”开始,同样操作。
D. 汽水和其他含CO2 的饮料:取100ml 样品,置于蒸发皿中。 水浴除去CO2后,移入250ml容量瓶中,用水洗涤蒸发皿,将洗涤液合并至容量瓶中,加水至刻度。 混合好,放在一边。
②测定:取处理后的样品溶液50ml置于400ml烧杯中,加入碱性酒石酸铜A溶液25ml和B溶液25ml,盖上表面皿,置于电炉上,在规定时间内加热至沸腾。 4分钟,然后准确煮2分钟。 趁热,用G4立式熔炼坩埚或内衬石棉的古什坩埚吸滤,用60℃热水洗涤烧杯和沉淀物,直至洗涤液不再呈碱性。 将古什坩埚或G4立式熔化坩埚放回400ml烧杯中,加入25ml Fe2(SO4)3溶液和25ml水,用玻璃棒搅拌至氧化亚铜完全溶解,用0.02mol/LKMnO4标准溶液滴定直至出现浅红色为终点。 。 同时吸取水50ml,加入与测试样品时等量的碱性酒石酸液A、B液、Fe2(SO4)3溶液和水,按同样方法做试剂空白试验。
5)结果计算
①根据滴定消耗的KMnO4标准溶液的体积,计算出相当于样品中还原糖的氧化亚铜的质量,即
m=(v-v0)×c×143.08×5/2=(v-v0)×c×357.7
式中,m——氧化亚铜的质量(mg)
v——测定样品溶液所消耗的KMnO4标准溶液的体积(ml)
v0——试剂空白试验消耗KMnO4标准溶液的体积(ml)
c——KMnO4标准溶液的浓度(mol/l)
143.08——氧化亚铜的摩尔质量(mg/m·mol)
②根据上式计算出的氧化亚铜的质量,查附录,得到还原糖的当量质量,然后根据式计算样品中还原糖的含量,即
w(还原糖)=m1×100/〔(1000×m×v2/v1)〕=m1×v1/(10×m×v2)
式中:w(还原糖)——还原糖的质量分数(%)
m——样品的质量(g)
m1——查表得到的还原糖当量质量(mg)
v1——样品处理液总体积(ml)
v2——测定用样品处理液体积(ml)
6) 说明
①注意反应条件的控制。 加入碱性酒石酸铜A、B后,必须控制在4分钟内沸腾,并维持沸腾2分钟。 时间必须准确,否则会造成误差大、重复性差。
② 如果在煮沸过程中溶液的蓝色消失,则说明糖度过高。 需减少样品处理液量并重新启动操作。 碱性酒石酸铜溶液的用量不宜增加。
③吸滤过程中,应防止氧化铜沉淀暴露在空气中,沉淀物应始终保持在液面以下,以免氧化。
④ 样品处理时,在碱性条件下使用CuSO4作为澄清剂,去除蛋白质等成分。
2 糕点、糖果中总糖的测定
总糖的测量通常基于测量还原糖的方法。 食品中的非还原性二糖被酸水解成还原性单糖,然后按照还原糖的测定方法进行测定。 测量以转化糖计算的总糖。 数量。
如果需要简单测定食品中的蔗糖量,可以测定水解前的还原糖量和水解后的还原糖量。 两者之差乘以修正系数0.95即可得到蔗糖量。 即1g转化糖的量相当于0.95g蔗糖的量。
在食品加工生产过程中,也常用相对密度法、折光法等简单的物理方法测定总糖含量。
一、原理
样品除去蛋白质后,加入稀HCl,在加热条件下将蔗糖水解成还原糖,然后用直接滴定法或高锰酸钾法测定。
2. 仪器
1)恒温水浴锅
2)其他仪器与还原糖测定相同
3. 试剂
1) 6mol/LHCl溶液
2)甲基红指示剂:称取0.1g甲基红,溶于100ml 60%(体积分数)乙醇中
3) 200g/LNaOH溶液
4)转化糖标准溶液:准确称取纯蔗糖1.0526g,溶于100ml水中。 将其置于带塞的锥形瓶中,加入5ml HCl(1:1),在68~70℃水浴中加热15分钟。 冷却至室温后,调整体积至1000ml。 每毫升该溶液相当于1.0毫克转化糖。
5) 其他试剂与还原糖测定相同
4. 测量方法
1)样品处理:按还原糖测定法中的方法进行。
2)样品中总糖含量的测定:取50ml样品处理液置于100ml容量瓶中,加入5ml 6mol/LHCl溶液,在68~70℃水浴中加热15min,冷却后,加入2滴甲基红指示剂。 用200g/L NaOH溶液中和至中性,加水至刻度,混匀,照还原糖测定法中的直接滴定法或高锰酸钾法测定。
5、结果计算
样品中总糖质量分数的计算公式为
w(总糖)=m1×100/[(1000×m×(50/v1)×(v2/100)]=m1×v1/(5×m×v2)
式中:w(总糖)——总糖的质量分数(%)
m——样品的质量(g)
m1——10ml碱性酒石酸铜相当于直接滴定法转化糖的质量(mg)

或查高锰酸钾法中表格,得到转化糖的当量质量(mg)
v1——样品处理液总体积(ml)
v2——测定总糖含量,取水解液体积(ml)
6. 说明
1) 分析结果的准确性和重现性取决于水解条件。 要求样品水解过程中,仅蔗糖被水解,其他化合物不被水解。
2)采用直接滴定法测定蔗糖时,为减少误差,必须用蔗糖标准溶液对碱性酒石酸铜溶液进行标定,蔗糖标准溶液应根据测定条件水解后进行标定。
3) 碱性酒石酸铜溶液的校准
①称取105℃干燥的纯蔗糖1.0000g,用蒸馏水溶解,转移至500ml容量瓶中,稀释至刻度,摇匀。 1ml该标准溶液相当于2mg纯蔗糖。
②取50ml蔗糖标准溶液置于100ml容量瓶中,加入5ml 6mol/LHCl溶液,在68~70℃水浴中加热15min,冷却后加2滴甲基红指示剂,用中和。 200g/LNaOH溶液至中性,加水至刻度,混匀。 1ml该标准溶液相当于1mg蔗糖。
③取水解蔗糖标准溶液,按直接滴定法校准碱性酒石酸铜溶液。 那么10ml碱性酒石酸铜溶液相当于转化糖的质量:
m2=v×m1/0.95
式中:m1——1ml蔗糖标准水解液相当于蔗糖的质量(mg)
m2——10ml碱性酒石酸铜溶液相当于转化糖的质量(mg)
v——校准时消耗的蔗糖标准水解液体积(ml)
0.95——蔗糖转化成转化糖的系数
4)酶法水解也可以利用酶的特异性进行,如利用β-果糖苷酶(转化糖)进行水解。 该方法应用的关键在于酶制剂本身的纯度和活性,目前很少使用。
3 糕点、糖果中蔗糖的测定
蔗糖是非还原性二糖,不能用还原糖的测定方法直接测定。 但蔗糖经酸水解后可生成还原性葡萄糖和果糖,然后可按照还原糖的测定方法进行测定。 对于纯度较高的蔗糖溶液,可采用相对密度、折射率、旋光度等物理测试方法进行测定。
一、原理
除去样品中的蛋白质和其他杂质后,用稀HCl水解,将蔗糖转化为还原糖。 然后按照还原糖的测定方法,测定水解前后样品溶液中还原糖的含量。 两者的差值就是蔗糖水解产生的还原糖的量,然后乘以换算系数0.95就是蔗糖的含量。
2. 试剂
1) 6mol/LHCl溶液。
2)甲基红指示剂:称取0.1g甲基红,溶于100ml 60%(体积分数)乙醇中。
3)200g/LNaOH溶液。
4)其他试剂同《糕点、糖果中还原糖的测定》。
3. 测量方法
取一定量的样品,按还原糖测定方法处理。 取处理后的样品两份各50ml,分别放入100ml容量瓶中。 其中一份加入5ml6mol/LHCl溶液,置于68~70℃水浴中加热15min。 取出并迅速冷却至室温。 加甲基红指示剂2滴,用200g/L NaOH溶液中和至中性,加水至刻度,混匀。 另一部分直接用水稀释至100ml。 通过直接滴定或高锰酸钾滴定测定还原糖。
4、结果计算
蔗糖质量分数的计算公式为
w(蔗糖)=(m2-m1)×0.95×100/[(1000×m×(50/v1)×(v2/100)]=(m2-m1)×0.19×v1/(m×v2)
式中:w(蔗糖)——蔗糖的质量分数(%)
m——样品的质量(g)
m1——样品溶液中未经水解的还原糖的质量(mg)
m2——样品溶液水解后还原糖的质量(mg)
v1——样品处理液总体积(ml)
v2——测定还原糖的样品处理液体积(ml)
0.95——还原糖还原成蔗糖的系数
5. 使用说明及注意事项
1)蔗糖在本法规定的水解条件下能完全水解。 必须严格控制水解条件,以确保结果的准确性和重现性。 另外,果糖在酸性溶液中易分解,因此水解后应立即取出并迅速冷却中和。
2)用还原糖法测定蔗糖时,为减少误差,测定的还原糖应以转化糖表示。 因此,采用直接法滴定时,必须根据测定条件,将蔗糖标准溶液水解后,进行碱性酒石酸铜溶液的标定。 校准,校准步骤为:
①称取105℃干燥的纯蔗糖1.000g,用蒸馏水溶解,定容至500ml,混匀。 1ml该标准溶液相当于2mg纯蔗糖。
②将50ml上述蔗糖标准溶液放入100ml容量瓶中,加入5ml 6mol/LHCl溶液,置于68~70℃水浴中加热15min,取出迅速冷却至室温,加入甲基红指示剂2滴,用200g/LNaOH溶液中和至中性,加水至刻度,混匀。 1ml该标准溶液相当于1mg纯蔗糖。
③ 取水解蔗糖标准溶液,按直接滴定法标定碱性酒石酸铜溶液。转化糖质量计算公式为
m2=v×m1/0.95
式中:m1——1ml蔗糖标准水解液相当于蔗糖的质量(mg)
m2——10ml碱性酒石酸铜溶液相当于转化糖的质量(mg)
v——校准时消耗的蔗糖标准水解液体积(ml)
0.95——蔗糖转化成转化糖的系数
3)如采用高锰酸钾滴定法,检查附录时应检查转化糖项目。
4 乳及乳制品中乳糖和蔗糖的测定
一、原理

从样品中除去蛋白质后,在加热条件下,以亚甲蓝为指示剂,直接用样品溶液滴定费林溶液。 当达到终点时,稍微过量的还原糖可以减少亚甲蓝指示剂的蓝色。 它变成无色。 根据样品溶液的消耗量,查乳糖和转化糖系数表,得到乳糖和蔗糖(用酸水解成转化糖)的含量。
2. 试剂
1)亚铁氰化钾溶液:称取10.6g亚铁氰化钾,加水溶解并稀释至100ml。
2)醋酸锌溶液:称取醋酸锌晶体21.9g,加冰醋酸3ml,加水溶解并稀释至100ml。
3)费林溶液(A溶液和B溶液)。
① A液:称取硫酸铜(CuSO4·5H2O)34.639g,加适量水溶解,加浓H2SO4 0.5ml,加水稀释至500ml,用精石棉过滤。
②B液:称取173g酒石酸钾钠和50g NaOH,加适量水溶解,稀释至500ml,用精石棉过滤,贮存于带橡皮塞的玻璃瓶中。
4)亚甲蓝(亚甲蓝)指示剂。
5) 6mol/LHCl溶液。
6)200g/LNaOH溶液。
7)20g/L甲基红乙醇溶液:称取0.2g甲基红,溶解于100ml 20%(体积分数)乙醇溶液中。
三、操作方法
1)样品处理:准确称取约3g样品置于小烧杯中,用100ml水溶解数次,洗入250ml容量瓶中。 缓慢加入醋酸锌溶液和亚铁氰化钾溶液各5ml,轻轻摇匀。 瓶子。 加水至刻度,静置几分钟,然后用干滤纸过滤,滤液备用。
2)乳糖的测定与计算
①测量
A、样品溶液的预先测定:取费林溶液A和溶液B各5ml,置于150ml锥形瓶中,加水10ml,加入玻璃珠2颗,控制在2分钟内沸腾,趁热,先快后慢。 逐滴添加样品溶液。 当颜色变浅时,加入2至3滴亚甲基蓝指示剂。 沸腾时,继续以 0.5 滴/秒的速度滴定,直至蓝色消失。 记录消耗的样品溶液的体积。
B、试样溶液的测定:取斐林溶液A和溶液B各5ml,置于150ml锥形瓶中,加水10ml,加入玻璃珠2颗,加入试样溶液约0.5~1ml,从滴定管进行粗滴定。 2分钟内加热沸腾,并维持沸腾2分钟。 加入2~3滴亚甲基蓝指示剂,以0.5滴/秒的速度继续滴定,同时沸腾,直至蓝色刚刚消失。 记录消耗的样品溶液的体积。
②结果计算
每100ml样品溶液中乳糖的质量(mg)为:
m1=100×m2/v
在公式:
m2——滴度对应的乳糖质量(mg)(详见下表)
v——滴定体积(ml)
如果蔗糖含量与乳糖含量之比超过3:1,则计算前应将下表末尾的修正值添加到效价中(一般加糖炼乳需要修正)。
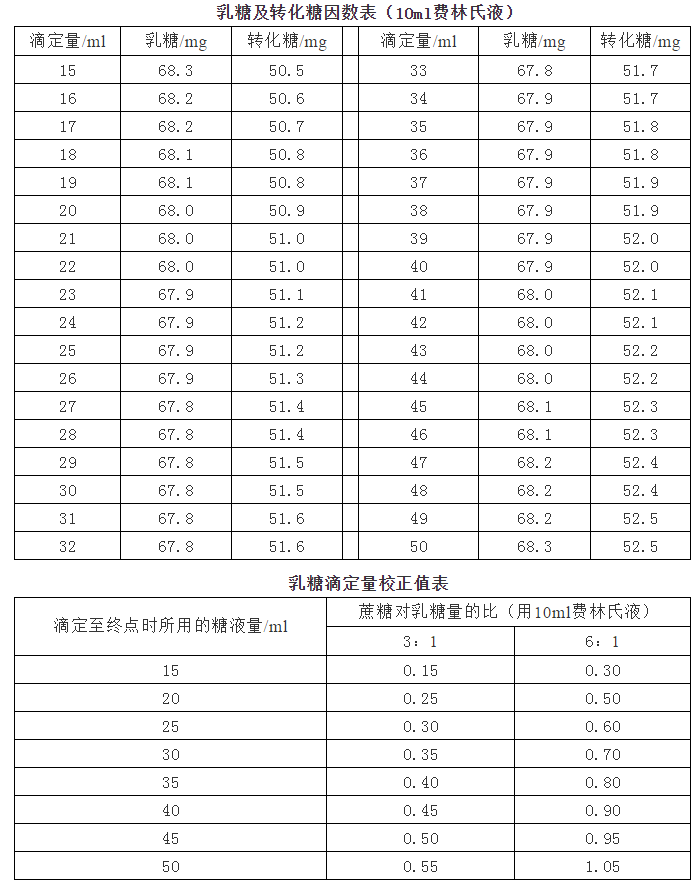
样品中乳糖的质量分数为:
w(乳糖)= m1 × 2.5 × 100/(1000 × m) = m1/(4 × m)
式中:w(乳糖)——乳糖的质量分数(%)
m——样品的质量(g)
m1——乳糖的质量(mg)
2.5——换算系数,即250/100
3)蔗糖的测定与计算
① 换算前转化糖的计算:用测定乳糖时的滴度,从上表中找出相应的转化糖系数,计算出100ml样品溶液中换算前转化糖的质量:
m1=100×m2/v
转化前转化糖的质量分数为
w(转化前的转化糖)= m1 × 2.5 × 100/(1000 × m) = m1/(4 × m)
式中:w(转化前转化糖)——转化前转化糖的质量分数(%)
m——样品的质量(g)
m1——100ml样品溶液换算前转化糖的质量(mg)
m2——对应效价的转化糖质量(mg)(见上表)
v——测量乳糖时的滴定体积(ml)
②样品溶液的换算与滴定:取糖提取液50ml,置于100ml容量瓶中,加入6mol/LHCl溶液5ml,置于68~70℃水浴中加热15min,取出,迅速冷却至室温,加2滴甲基红为指示剂,用200g/L NaOH溶液中和至微酸性,加水至刻度,混匀。
滴定方法与乳糖测定相同,由滴定体积可计算出换算后每100ml样品溶液中转化糖的质量,即
m1=100×m2/v
换算后转化糖的质量分数为
w(换算糖)=m1×5×100/(1000×m)=m1/(2×m)
③蔗糖质量分数的计算公式为:
w(蔗糖)=[w(转化后的转化糖)-w(转化前的转化糖)]×0.95
4) 使用说明及注意事项
①测定乳及乳制品中乳糖和蔗糖的含量,也可采用测定糕点、糖果中还原糖和蔗糖的相同方法。
②斐林A液和B液应分别配制和保存,使用前等量混合,以免Cu(OH)2在碱性溶液中被酒石酸钾、酒石酸钠缓慢还原,从而析出少量CuO,降低有效浓度。 。
③ 该方法中需要用乳糖和蔗糖(分析纯)校准费林溶液。



